Javen – Chất tẩy là gì?
 Bạn thường thấy các chai chất tẩy rửa quần áo nhà vệ sinh, phòng tắm, nhà bếp trong gia đình mình. Chúng dùng để khử trùng, làm sáng bề mặt, hoặc tảy màu… vậy chất đó là gì được cấu tạo như thế nào.
Bạn thường thấy các chai chất tẩy rửa quần áo nhà vệ sinh, phòng tắm, nhà bếp trong gia đình mình. Chúng dùng để khử trùng, làm sáng bề mặt, hoặc tảy màu… vậy chất đó là gì được cấu tạo như thế nào.
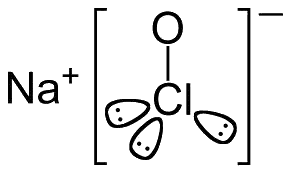
Chất tẩy Javen là một hỗn hợp các hoá chất, thành phần chính của nó là dung dịch natri hypochlorite (NaOCl) ~ 3-6%, được trộn với một lượng nhỏ natri hydroxit (NaOH), hydrogen peroxide (H2O2) và calcium hypochlorite(Ca(ClO)2).
Javen – Sodium hypochlorite cũng được sử dụng trên quy mô lớn trong nông nghiệp, và các ngành công nghiệp như hóa chất, sơn, vôi, thực phẩm, thủy tinh, giấy, dược phẩm, tổng hợp và xử lý chất thải. Javen thường được thêm vào nước thải công nghiệp để giảm mùi, vì NaOCl trung hòa H2S và amoniac. Javen cũng được sử dụng để khử độc các dung dịch Xyanua được sử dụng trong quá trình mạ kim loại, và để ngăn ngừa tảo và sự phát triển của vỏ tôm ở các tháp làm mát. Ngoài ra Javen cũng được sử dụng để làm sạch nguồn nước và bể bơi.
Javen được phát minh khi nào?
Chất tẩy lỏng dựa trên natri hypochlorite được Claude Louis Berthollet người Pháp vào năm 1785. Sau đó nó được giới thiệu rộng rãi bởi Công ty sản xuất Javel dưới cái tên liqueur de Javel . Ban đầu, nó được sử dụng để tẩy bông, nhưng sớm trở thành một hợp chất phổ biến để tẩy trắng các vật liệu quần áo khác vì nó đã nhanh chóng phát hiện ra rằng hypochlorite natri có thể loại bỏ vết bẩn từ quần áo ở nhiệt độ phòng. Ở Pháp, Natri hypochlorite vẫn còn được gọi là eau de Javel.
Do đó nguồn gốc chữ Javen (Giaven) ngày nay chúng ta hay dùng có trong tiếng Việt có nguồn từ eau de Javel trong tiếng Pháp.
Hình dạng của Javen?

Javen được tạo ra như thế nào?
Một phương pháp sản xuất có hiệu quả hơn đã được ES Smith phát minh ra trong thập niên 1890 của các nhà khoa học liên quan đến việc thẩm tách dung dịch muối để tạo ra NaOH và khí Cl 2, sau đó đã được trộn lẫn với nhau để tạo ra NaOCl. Ngày nay, phương pháp công nghiệp lớn duy nhất để sản xuất NaOCl được gọi là quá trình Hooker, và chỉ là một phiên bản cải tiến của quá trình điện phân của Smith. Trong đó, khí Cl2 được đưa vào dung dịch NaOH pha loãng, tạo thành NaOCl, với NaCl làm sản phẩm chính. Phản ứng mất cân bằng (Cl 2 là đồng thời oxy hóa và giảm) được thúc đẩy để hoàn thành bằng điện phân, và hỗn hợp phải được giữ dưới 40°C để ngăn chặn sự hình thành không mong muốn natri clorat.
Javen hoạt động như thế nào?
Javen có tính ô xi hóa mạnh nên dễ phản ứng và thực sự không ổn định. Ở nhiệt độ phòng khí clo sẽ bốc hơi từ dung dịch với tốc độ đáng kể, và nếu nó được làm nóng, NaClO sẽ phân hủy tạo thành muối và oxy. Điều này cũng xảy ra khi tiếp xúc với axit, ánh sáng mặt trời, kim loại nhất định, và một vài khí.
Đây cũng là lý do tại sao chất tẩy có thể được sử dụng trên quy mô lớn vì ngay sau khi sử dụng nó phân hủy thành các sản phẩm lành tính (muối và nước). Javen có thể được đổ trực tiếp vào hệ thống thoát nước mà không có vấn đề.
Chất tẩy rửa cũng hoạt động theo một số phương pháp. Các axit hypochlorous (HOCl) thành phần là một tác nhân oxy hoá rất mạnh (thậm chí mạnh hơn Cl 2 khí), và có thể phản ứng với và tiêu diệt nhiều loại phân tử, bao gồm thuốc nhuộm. Ngoài ra, ion hypochlorit phân hủy thành Clorua và một dạng oxy phản ứng cao:
2ClO – —-> 2Cl – + O 2
Các HOCl (và để mở rộng các Cl 2 và oxy hoạt động) sau đó có thể tấn công các liên kết hóa học trong một hợp chất màu, hoàn toàn phá hủy chromophore (một phần của phân tử đó cho nó màu sắc của nó), hoặc chuyển đổi các liên kết đôi trong các chromophore, do đó ngăn chặn các phân tử hấp thụ ánh sáng nhìn thấy.
Khi nó phản ứng với các vi khuẩn, NaCLO tấn công các protein trong tế bào khiến cho các protein hòa trộn và các vi khuẩn kết tụ lại và chết. Nó cũng có thể gây ra màng tế bào vỡ. Cuộc tấn công phổ rộng này làm thuốc tẩy có hiệu quả chống lại một phạm vi rộng của vi khuẩn. Natri hypochlorite là chất kiềm, và chất tẩy gia đình cũng chứa NaOH để làm cho dung dịch trở nên kiềm hơn. Hai chất được hình thành khi natri hypochlorite hoà tan trong nước. Đó là các axit hypochlorous (HOCl) và ion hypochlorite (OCl – ), với tỷ lệ giữa hai được xác định bởi độ pH của nước.




