Hidrocacbon là gì? Hidrocacbon là một hợp chất hữu cơ quen thuộc trong bộ môn hóa học và cũng là một chất có nhiều ứng dụng trong cuộc sống. Trong bài viết ngày hôm nay, chúng tôi sẽ chia sẻ đến bạn đọc những thông tin về tính chất, cách sản xuất và ứng dụng của các loại hidrocabon.
Hidrocacbon là gì

Hidrocacbon là gì
Hidrocacbon là một loại hợp chất hữu cơ mà trong cấu tạo chỉ có cacbon (C) và hidro (H). Chúng có thể liên kết với nhau bằng các liên kết 1, 2 hoặc 3.
Dựa vào liên kết của các nguyên tử C và H mà hiđrocacbon được chia làm 3 loại như sau:
- Hidrocacbon no: Trong phân tử chỉ có 1 liên kết đơn, gồm 2 nhóm chính đó là ankan và cycloankan.
- Hidrocacbon không no: Trong phân tử có các liên kết đôi hoặc ba và nó được chia ra làm 3 nhóm chính là anken (có 1 liên kết đôi), ankadien (có 2 liên kết đôi) và ankin (có 1 liên kết ba).
- Hidrocacbon thơm: Các nguyên tử C liên kết khép kín tạo thành vòng.
Chi tiết về các loại hidrocabon
Hidrocacbon no
Hidrocarbon no là các hidrocarbon mà các nguyên tử C trong phân tử của nó liên kết lại với nhau bằng liên kết đơn. Những hóa trị còn lại được sẽ bão hòa bởi các nguyên tử hydrogen.
Hidrocarbon no gồm 2 loại là alkane (paraffin) và cycloalkane
Ankane
Ankane (ankan) là các hidrocacbon không tạo mạch vòng và trong mỗi phân tử đều có chứa số nguyên tử hidro cực đại, đồng thời không chứa các liên kết đôi. Công thức chung của ankane là CnH2n+2 (n≥1).
– Tên gọi:
- Tên thay thế của ankan: Số chỉ vị trí nhánh + tên nhánh + mạch nhánh chính + đuôi “an”
- Tên thông thường: Nếu chỉ có một nhánh CH3 duy nhất ở nguyên tử C số 2 thì thêm tiền tố “iso”, còn nếu có 2 nhánh CH3 ở nguyên tử C số 2 thì thêm tiền tố “neo”.
– Tính chất vật lý
- Ở nhiệt độ thường, các ankan từ C1 – C4 ((như metan, etan, propan và butan) tồn tại ở trạng thái khí, từ C5 – C10 (như hexan, heptan, octan,…) là trạng thái lỏng và từ khoảng C10 trở lên là trạng thái rắn.
- Ankan có khả năng cách điện tốt và nó kém hòa tan trong nước nhưng tan tốt trong các dung môi hữu cơ.
- Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng của ankan nói chung đều tăng theo số lượng nguyên tử C có trong phân tử (tăng theo phân tử khối).
– Tính chất hóa học
Ankan là hợp chất hữu cơ bão hòa nên nó khá trơ với nhiều phản ứng hóa học. Tuy nhiên, nó có thể tham gia vào các phản ứng như phản ứng halogen hóa, phản ứng đốt cháy và phản ứng cắt.
- Phản ứng halogen hóa
Clo có thể thay thế lần lượt các nguyên tử hydro trong phân tử CH4 , sản phẩm thế ưu tiên với hydro ở C bậc cao.
Cl2 + CH4 → CH3Cl + HCl
Cl2 + CH3Cl → CH2Cl2 + HCl
Cl2 + CH2Cl2 → CHCl3 + HCl
Cl2 + CHCl3 → CCl4 + HCl
- Phản ứng tách hydro để hydro hóa
- Phản ứng cracking hay chính là phản ứng bẻ gãy mạch cacbon
- Phản ứng oxi hóa hoàn toàn
CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n+1)H2O
Ví dụ như CH4 + 2O2 → CO2 + 2H2O
– Điều chế Ankan
Tùy từng điều kiện mà ankan sẽ được điều chế từ các cách khác nhau như:
- Phòng thí nghiệm (có xúc tác Pt, Ni hoặc Pd và đun nóng): CnH2n +H2 → CnH2n+2
- Trong công nghiệp: Metan và các đồng đẳng của nó được tách từ khí thiên nhiên và dầu mỏ thông qua quy trình tinh chế và cải tạo. Chúng cũng có thể được tạo ra từ các phản ứng giữa những hợp chất hữu cơ khác như halogenua và alcancol.
– Ứng dụng
Hidrocacon từ C1 – C20 được ứng dụng làm nhiên liệu và điều chế chất sinh hàn. Dưới tác dụng của nhiệt và các phản ứng oxi hóa không hoàn, các sản phẩm như HCHO, rượu metylic, axit axetic,… sẽ được tạo thành. Ngoài ra, nhiều ankan còn được sử dụng làm dầu bôi trơn máy và dung môi hữu cơ.
Xicloankan
Xicloankan là những hidrocacbon no mạch vòng và trong phân tử chỉ chứa liên kết đơn. Nó có công thức tổng quát là CnH2n (n≥3).
– Tên gọi
Tên gọi của xicloankan sẽ là: Số chỉ vị trí nhánh + tên nhánh + “xiclo” + tên mạch chính + đuôi “an”.
– Tính chất vật lý
- Các xicloankan nhẹ tồn tại ở dạng khí trong điều kiện nhiệt độ và áp suất phòng
- Các xicloankan có trọng lượng phân tử cao hơn tồn tại ở dạng lỏng.
- Các xicloankan có trọng lượng phân tử rất lớn tồn tại ở dạng rắn.
- Các xicloankan không tan trong nước nhưng tan tốt trong các dung môi hữu cơ.
– Tính chất hóa học
Tính chất hóa học của xicloankan tương tự như các ankan tuyến tính tương ứng của chúng nhưng có một số sự khác biệt do căng co lập thể.
- Phản ứng thế
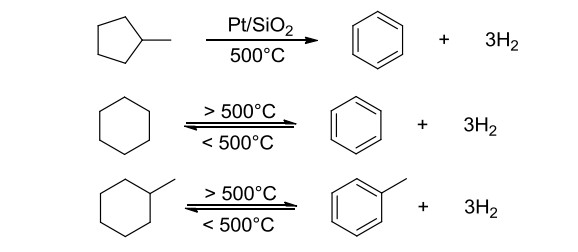
Khi ở nhiệt độ cao > 500°C và có mặt xúc tác (Pt, Ni, …), xicloankan bị đề hidro hóa thành hidrocacbon thơm. Phản ứng này được sử dụng trong phương pháp reforming để gia tăng chỉ số octan hoặc sản xuất hidrocacbon thơm (benzen, xilen, toluen, …).
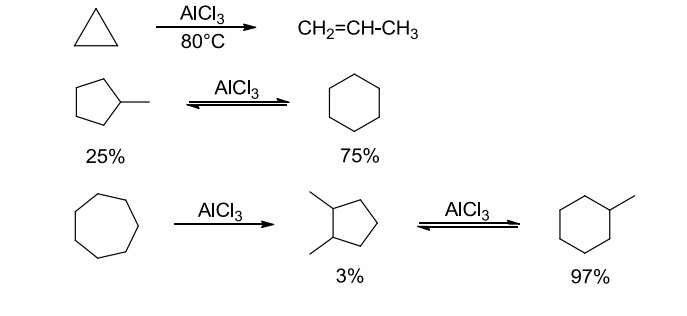
– Khi có xúc tác là AlCl3 hoặc AlBr3, xiclopropan sẽ bị đồng phân hóa thành propen còn các xicloankan khác bị đồng phân hóa thành vòng 6 cạnh bền hơn.
- Phản ứng cộng mở vòng
Xiclopropan tham gia phản ứng cộng mở vòng 3,4 như anken:
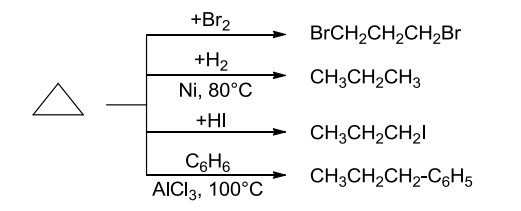
Xiclobutan chỉ tham gia phản ứng cộng mở vòng trong điều kiện nhiệt độ cao hơn xiclopropan và không xảy ra phản ứng với các tác nhân còn lại.
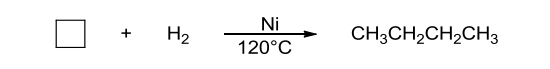
Các vòng từ 5 cạnh trở lên không có sức căng nội phân tử lớn nên chúng tham gia phản ứng giống như là ankan mạch hở. Chúng chỉ bị hidro hóa mở vòng khi ở nhiệt độ rất cao, trên > 500°C và có chất xúc tác.
– Điều chế
Xicloankan có trong dầu mỏ (khoảng 30 ÷ 60%) dưới dạng vòng 5, 6 cạnh với các nhánh từ 1 đến hàng chục nguyên tử cacbon, ngoài ra còn có các polixicloankan 2,3,4 hoặc 5 vòng (hidrocacbon naphtenic). Khi chưng cất dầu mỏ, xicloankan vòng 5,6 cạnh sẽ được thu ở phân đoạn sôi với nhiệt độ 60 – 90°C. Từ phân đoạn này, xiclohexan, metylxiclopentan, … có thể được thu lại và dùng trong công nghiệp.
Ngoài ra, chúng ta cũng có thể điều chế xicloankan bằng cách tác dụng với H2 và đóng vòng ankan.
– Ứng dụng
Hidrocacbon naphtenic là thành phần quan trọng trong dầu nhờn và nhiên liệu động cơ. Nó là nguồn nguyên liệu quý cho tổng hợp hữu cơ, ví dụ như xiclohexan từ phân đoạn sôi ở 60 – 90°C là nguyên liệu quan trọng trong quá trình tổng hợp nilon-6 và nilon-6,6.
Xiclohexan và đồng đẳng của nó còn được dùng để sản xuất benzen, toluene, xilen. Một số xicloankan như xiclohexan có thể là chất gây ung thư.
Hidrocacbon không no
Hidrocacbon không no là hidrocacbon có chứa ít nhất 1 liên kết đôi trở lên trong cấu trúc phân tử của nó, tuy nhiên trong phân tử phải của hidrocacbon không no không có mạch vòng như hidrocacbon thơm, mà chỉ có dạng mạch phân nhánh hoặc mạch thẳng.
Hidrocacbon không no được phân loại thành 3 loại chính là:
- Anken (chứa 1 liên kết đôi): CnH2n với n≥2
- Ankadien (chứa 2 liên kết đôi): CnH2n-2 với n≥3.
- Ankin (có 1 liên kết 3): CnH2n-2 với n≥2.
- Dạng hỗn hợp của ba dạng trên.
Ngoài ra, một số hidrocacbon không no có chứa liên kết đôi còn chia thành những đồng phân cis-trans do những nhóm này có liên kết đôi khác nhau ở mỗi một bên. Vậy nên khi quay quanh mặt phẳng chứa liên kết đôi, nó sẽ trở thành các dạng khác nhau.
– Tính chất hóa học
- Phản ứng với hidro tạo thành hidrocacbon no nếu là hidro hóa hoàn toàn
H2 + C3H6 → C3H8
2H2+C3H4→C3H8
- Phản ứng oxi hóa: Phản ứng cháy, anđehit hóa, ancol hóa,…
CnH2n + (3n/2)O2 → nCO2 + nH2O
CnH2n-2 +((3n-1)/2)O2 → nCO2 + (n-1)H2O
- Phản ứng với HCl tạo ra các chất dẫn xuất halogen
HCl + C3H6 → C3H7Cl
CH≡CH+HCl → CH2=CHCl
– Ứng dụng
Anken được ứng dụng trong sản xuất keo dán, sản xuất chất dẻo PVC, PE, nguyên liệu hóa học, sản xuất axit hữu cơ,…
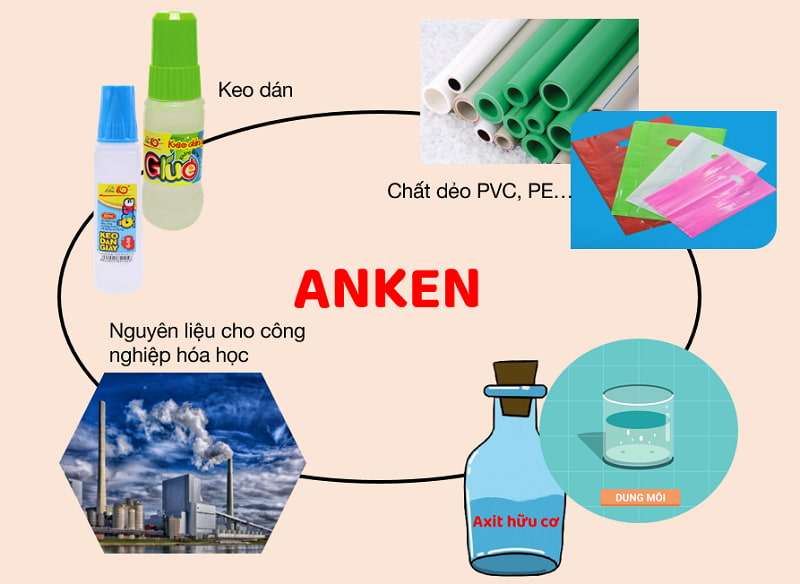
Ứng dụng của anken
Hidrocacbon thơm
Hidrocacbon thơm là hidrocacbon mà trong phân tử của nó gồm các nguyên tử C khép kín. Trong điều kiện nhiệt độ phòng, hidrocacbon thơm là chất lỏng hoặc rắn có nhiệt độ sôi tăng theo phân tử khối. Benzen và ankylbenzen là những chất không màu, không tan trong nước nhưng tan mạnh trong các dung môi hữu cơ, có mùi đặc trưng.
Hidrocacbon thơm gồm có
- Benzen và đồng đẳng của benzene: Benzen và các hidrocacbon thơm khác lập thành dãy đồng đẳng có công thức phân tử chung là CnH2n-6 (n≥6).
- Hidrocacbon thơm có nhiều nhân có cấu trúc phức tạp hơn với nhiều vòng benzen trong phân tử.
- Hidrocacbon thơm không chứa vòng benzene mà chứa những vòng khác.
– Tính chất hóa học
- Phản ứng thế nguyên tử hidro của vòng benzene có xúc tác bột sắt.
- Phản ứng oxi hóa không hoàn toàn
- Phản ứng cộng
– Điều chế
Benzen, toluen, xilen thường tách bằng cách chưng cất nhựa than đá, dầu mỏ hoặc điều chế từ ankan và xicloankan
– Ứng dụng
Sản xuất dung môi, thuốc nổ TNT, phẩm nhuộm, sản xuất dược phẩm, polime,….
Trên đây là những thông tin về hidrocacbon là gì mà chúng tôi muốn chia sẻ đến bạn đọc. Hy vọng bài viết này sẽ đem lại cho bạn những kiến thức hữu ích để áp dụng trong học tập và cuộc sống. Đừng quên liên hệ với khi có nhu cầu mua hóa chất xử lý nước như PAC, Javel,… bạn nhé.




